As mutações génicas podem produzir mudanças positivas nos seres vivos?
Os evolucionistas têm sustentado que as mutações génicas são uma estrada de mudanças positivas nos organismos vivos. Por exemplo, o livro de Richard Dawkins, The Blind Watchmaker (O Relojoeiro Cego), busca estabelecer um universo de acasos, sem Deus, em que o aparecimento de design na vida ocorreu por acidente, por sucessivos acúmulos de mudanças positivas nos genes. Sua evidência relacionada à genética bioquímica, contudo, consiste em modelos teóricos de pequena relevância no mundo real.
(…)
(…)
O problema das mutações humanas é ruim e está ficando pior.
Literalmente milhares de doenças humanas associadas a mutações  genéticas têm sido catalogadas nos últimos anos, com mais sendo descritas continuamente. Um livro recente de referência em genética médica listou umas 4.500 doenças genéticas diferentes. Algumas das síndromes hereditárias caracterizadas clinicamente antes das análises das moléculas dos genes (tais como a síndrome de Marfan) agora têm demonstrado ser heterogêneas; ou seja, associadas a muitas mutações diferentes. Esta revisão vai apenas arranhar a superfície das muitas descobertas recentes. Ainda assim, os exemplos citados irão ilustrar um princípio geral convincente que se estende por todo esse campo em expansão.
genéticas têm sido catalogadas nos últimos anos, com mais sendo descritas continuamente. Um livro recente de referência em genética médica listou umas 4.500 doenças genéticas diferentes. Algumas das síndromes hereditárias caracterizadas clinicamente antes das análises das moléculas dos genes (tais como a síndrome de Marfan) agora têm demonstrado ser heterogêneas; ou seja, associadas a muitas mutações diferentes. Esta revisão vai apenas arranhar a superfície das muitas descobertas recentes. Ainda assim, os exemplos citados irão ilustrar um princípio geral convincente que se estende por todo esse campo em expansão.
 genéticas têm sido catalogadas nos últimos anos, com mais sendo descritas continuamente. Um livro recente de referência em genética médica listou umas 4.500 doenças genéticas diferentes. Algumas das síndromes hereditárias caracterizadas clinicamente antes das análises das moléculas dos genes (tais como a síndrome de Marfan) agora têm demonstrado ser heterogêneas; ou seja, associadas a muitas mutações diferentes. Esta revisão vai apenas arranhar a superfície das muitas descobertas recentes. Ainda assim, os exemplos citados irão ilustrar um princípio geral convincente que se estende por todo esse campo em expansão.
genéticas têm sido catalogadas nos últimos anos, com mais sendo descritas continuamente. Um livro recente de referência em genética médica listou umas 4.500 doenças genéticas diferentes. Algumas das síndromes hereditárias caracterizadas clinicamente antes das análises das moléculas dos genes (tais como a síndrome de Marfan) agora têm demonstrado ser heterogêneas; ou seja, associadas a muitas mutações diferentes. Esta revisão vai apenas arranhar a superfície das muitas descobertas recentes. Ainda assim, os exemplos citados irão ilustrar um princípio geral convincente que se estende por todo esse campo em expansão.O que são mutações?
Mutações são definidas como alterações aleatórias no DNA celular. Elas mudam o código genético que determina a sequência dos aminoácidos nas proteínas, introduzindo assim erros bioquímicos de graus de severidade variáveis. As mutações têm sido classificadas como delecções (perda de bases do DNA), inserções (ganho de bases do DNA), e translocações (substituição de uma base do DNA).
Se as mutações afectam as células germinativas (óvulo feminino e espermatozóide masculino), elas são transmitidas para todas as células dos descendentes, e afectam as gerações futuras. Tais mutações são denominadas "mutações germinativas", e são a causa de doenças hereditárias.
As mutações também ocorrem em outras populações de células do corpo e vão se acumulando durante o período de vida, sem ser transmitidas aos descendentes. Estas são as chamadas "mutações somáticas", e são importantes na origem de cânceres e outros processos de doenças degenerativas.
(…)
Mutações são definidas como alterações aleatórias no DNA celular. Elas mudam o código genético que determina a sequência dos aminoácidos nas proteínas, introduzindo assim erros bioquímicos de graus de severidade variáveis. As mutações têm sido classificadas como delecções (perda de bases do DNA), inserções (ganho de bases do DNA), e translocações (substituição de uma base do DNA).
Se as mutações afectam as células germinativas (óvulo feminino e espermatozóide masculino), elas são transmitidas para todas as células dos descendentes, e afectam as gerações futuras. Tais mutações são denominadas "mutações germinativas", e são a causa de doenças hereditárias.
As mutações também ocorrem em outras populações de células do corpo e vão se acumulando durante o período de vida, sem ser transmitidas aos descendentes. Estas são as chamadas "mutações somáticas", e são importantes na origem de cânceres e outros processos de doenças degenerativas.
(…)
Mutações relacionadas ao colesterol
No sistema cardiovascular, há muito tempo se reconhece que um elevado conteúdo de colesterol circulando no sangue está associado com a degeneração e o estreitamento de artérias médias e grandes. Este processo é denominado "arteriosclerose" e é uma das principais causas de doenças do coração. Mais recentemente, um defeito bioquímico genético causador de altos níveis hereditários de colesterol no sangue foi descoberto e é conhecido como "hipercolesterolemia familiar" (FH).
Essa desordem tem sido relacionada à mutação de um gene que codifica uma proteína receptora da membrana celular. O gene está no cromossoma 19 e tem cerca de 45.000 pares de bases com 18 exons (códigos para a molécula de RNA mensageiro). Sua proteína receptora codificada está ancorada nas membranas de todas as células do corpo, e permite-lhes capturarem e absorverem "pacotes" de gordura e colesterol (chamados lipoproteínas de "baixa densidade" - "low-density lipoproteins", ou LDL) que são fabricados no fígado. A proteína receptora tem 772 aminoácidos que formam cinco domínios funcionais.
Pelo menos 350 diferentes mutações do receptor de colesterol, causadoras de doenças, têm sido descritas. Elas podem ser classifica das de acordo com o domínio funcional afectado.
No sistema cardiovascular, há muito tempo se reconhece que um elevado conteúdo de colesterol circulando no sangue está associado com a degeneração e o estreitamento de artérias médias e grandes. Este processo é denominado "arteriosclerose" e é uma das principais causas de doenças do coração. Mais recentemente, um defeito bioquímico genético causador de altos níveis hereditários de colesterol no sangue foi descoberto e é conhecido como "hipercolesterolemia familiar" (FH).
Essa desordem tem sido relacionada à mutação de um gene que codifica uma proteína receptora da membrana celular. O gene está no cromossoma 19 e tem cerca de 45.000 pares de bases com 18 exons (códigos para a molécula de RNA mensageiro). Sua proteína receptora codificada está ancorada nas membranas de todas as células do corpo, e permite-lhes capturarem e absorverem "pacotes" de gordura e colesterol (chamados lipoproteínas de "baixa densidade" - "low-density lipoproteins", ou LDL) que são fabricados no fígado. A proteína receptora tem 772 aminoácidos que formam cinco domínios funcionais.
Pelo menos 350 diferentes mutações do receptor de colesterol, causadoras de doenças, têm sido descritas. Elas podem ser classifica das de acordo com o domínio funcional afectado.
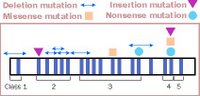
Na primeira classe de mutação, pouco ou nenhum receptor é sintetizado. Na segunda, a proteína receptora é sintetizada, mas não toma seu devido lugar na membrana celular. Na terceira, a proteína receptora está presente na membrana mas não se liga aos pacotes de LDL. Na quarta, a proteína receptora é incapaz de permanecer na membrana. Na quinta, a proteína receptora está presente na membrana e se liga aos pacotes de LDL, mas não os transporta para o interior da célula. Nenhuma dessas é benéfica.
Todas as células do corpo necessitam de colesterol para suas membranas; então, uma certa quantidade é necessária e benéfica. Contudo, defeitos nesse receptor de proteína resultam em altos níveis de colesterol no sangue através de um ciclo de retroalimentação (feedback). Quando o receptor de proteína não está funcionando, as células continuam enviando os sinais para a fabricação de mais pacotes de colesterol, e o fígado obedece. Em homozigotos, os níveis de colesterol são de três a cinco vezes o nível adequado, enquanto heterozigotos têm cerca de duas vezes o nível adequado. Isso resulta em uma rápida arteriosclerose, que às vezes resulta em doenças cardíacas fatais na infância.
Todas as células do corpo necessitam de colesterol para suas membranas; então, uma certa quantidade é necessária e benéfica. Contudo, defeitos nesse receptor de proteína resultam em altos níveis de colesterol no sangue através de um ciclo de retroalimentação (feedback). Quando o receptor de proteína não está funcionando, as células continuam enviando os sinais para a fabricação de mais pacotes de colesterol, e o fígado obedece. Em homozigotos, os níveis de colesterol são de três a cinco vezes o nível adequado, enquanto heterozigotos têm cerca de duas vezes o nível adequado. Isso resulta em uma rápida arteriosclerose, que às vezes resulta em doenças cardíacas fatais na infância.
Mutação da fibrose cística
Um segundo exemplo é uma doença genética comum, a fibrose cística (FC). Esta doença afecta muitos sistemas e aleija crianças, levando à morte prematura. Ela danifica os pulmões, os órgão digestivos e, nos homens, os vasos deferentes (dutos espermáticos). Seus diferentes efeitos, de brandos a severos, são em parte devido a diferentes tipos de mutação afectando um gene chave.
Essa base bioquímica é a mutação de um gene codificador de uma proteína da membrana que regula o transporte de iões cloreto através da membrana celular. Esse gene tem 250.000 pares de bases e é denominado de gene CFTR. Ele codifica uma proteína da membrana composta de 1.480 aminoácidos. Pesquisas sobre esse gene mostraram uma mutação, delta-F508, ocorrendo na maioria dos casos clínicos de FC. Essa mutação é uma delecção de três nucleotídeos resultando na perda de resíduo de fenilalanina na posição 508 da cadeia de peptídeos.
Um segundo exemplo é uma doença genética comum, a fibrose cística (FC). Esta doença afecta muitos sistemas e aleija crianças, levando à morte prematura. Ela danifica os pulmões, os órgão digestivos e, nos homens, os vasos deferentes (dutos espermáticos). Seus diferentes efeitos, de brandos a severos, são em parte devido a diferentes tipos de mutação afectando um gene chave.
Essa base bioquímica é a mutação de um gene codificador de uma proteína da membrana que regula o transporte de iões cloreto através da membrana celular. Esse gene tem 250.000 pares de bases e é denominado de gene CFTR. Ele codifica uma proteína da membrana composta de 1.480 aminoácidos. Pesquisas sobre esse gene mostraram uma mutação, delta-F508, ocorrendo na maioria dos casos clínicos de FC. Essa mutação é uma delecção de três nucleotídeos resultando na perda de resíduo de fenilalanina na posição 508 da cadeia de peptídeos.
Além dessa mutação geralmente comum, mais de 200 outras mutações desse gene foram descritas. Apenas algumas poucas dessas estão associadas às formas mais severas da doença, que levam à morte prematura por infecções pulmonares. Outras mutações ou combinações de mutações levam a estados menos graves da doença, como pancreatite crónica ou esterilidade masculina, mas, novamente, nenhum resultado benéfico tem sido observado.
Câncer
Como um exemplo abrangente de doença produzida por mutações somáticas, vamos considerar o câncer. A ligação entre as causas de câncer e mutações genéticas tem se tornado muito mais clara.
Cancerígenos (agentes que causam câncer) também tendem a ser poderosos mutagénicos (agentes que produzem mutações). A descoberta de "oncogenes" e "genes supressores de tumor" tem demonstrado como essa relação funciona. Basicamente, esses genes estão envolvidos com a regulação do ciclo celular. Os oncogenes forçam a reprodução da célula para adiante, enquanto os genes supressores de tumor a detêm. Ambos são necessários para o funcionamento adequado e o crescimento da célula. Mas danos causados por mutação aos componentes de ambos os sistemas podem produzir um crescimento descontrolado das células, ou seja, câncer.
Este fenómeno pode ser comparado a um carro em que há danos no acelerador, fazendo com que ele fique preso "acelerando", enquanto os freios também estão danificados. Essas mutações são normalmente adquiridas ao longo de décadas, assim o câncer é principalmente uma doença da velhice. Contudo, estudos mostram que mutações germinativas herdadas, nos oncogenes e genes supressores chaves podem predispor pessoas ao desenvolvimento de câncer na infância.
Exemplos disso incluem câncer na infância como retinoblastoma, assim como casos hereditários de câncer mais comuns (por exemplo, na mama ou no cólon) que estão ligados a genes mutantes específicos (por exemplo, o BRCA1 e BRCA2 para câncer de mama hereditário, e o gene APC para câncer e pólipos hereditários no cólon).
(…)
Como um exemplo abrangente de doença produzida por mutações somáticas, vamos considerar o câncer. A ligação entre as causas de câncer e mutações genéticas tem se tornado muito mais clara.
Cancerígenos (agentes que causam câncer) também tendem a ser poderosos mutagénicos (agentes que produzem mutações). A descoberta de "oncogenes" e "genes supressores de tumor" tem demonstrado como essa relação funciona. Basicamente, esses genes estão envolvidos com a regulação do ciclo celular. Os oncogenes forçam a reprodução da célula para adiante, enquanto os genes supressores de tumor a detêm. Ambos são necessários para o funcionamento adequado e o crescimento da célula. Mas danos causados por mutação aos componentes de ambos os sistemas podem produzir um crescimento descontrolado das células, ou seja, câncer.
Este fenómeno pode ser comparado a um carro em que há danos no acelerador, fazendo com que ele fique preso "acelerando", enquanto os freios também estão danificados. Essas mutações são normalmente adquiridas ao longo de décadas, assim o câncer é principalmente uma doença da velhice. Contudo, estudos mostram que mutações germinativas herdadas, nos oncogenes e genes supressores chaves podem predispor pessoas ao desenvolvimento de câncer na infância.
Exemplos disso incluem câncer na infância como retinoblastoma, assim como casos hereditários de câncer mais comuns (por exemplo, na mama ou no cólon) que estão ligados a genes mutantes específicos (por exemplo, o BRCA1 e BRCA2 para câncer de mama hereditário, e o gene APC para câncer e pólipos hereditários no cólon).
(…)
Anemia Falciforme
A mutação responsável pela anemia falciforme foi apresentada como um exemplo de Evolução. Isso é obviamente problemático, visto que a mutação falciforme, como muitas outras mutações descritas da hemoglobina, claramente prejudica a função da outrora maravilhosamente bem-formada molécula de hemoglobina. De maneira nenhuma ela pode ser considerada como uma melhoria em nossa espécie, mesmo que sua preservação seja aumentada pela selecção natural em áreas da África central onde a malária é endémica.
A mutação responsável pela anemia falciforme foi apresentada como um exemplo de Evolução. Isso é obviamente problemático, visto que a mutação falciforme, como muitas outras mutações descritas da hemoglobina, claramente prejudica a função da outrora maravilhosamente bem-formada molécula de hemoglobina. De maneira nenhuma ela pode ser considerada como uma melhoria em nossa espécie, mesmo que sua preservação seja aumentada pela selecção natural em áreas da África central onde a malária é endémica.
Degeneração de células cancerosas
Ainda mais estranhamente, o processo de degeneração de células cancerosas tem sido visto como uma forma Darwiniana de mutação Mais uma vez, essa ideia falha em se sustentar quando submetida a um exame mais minucioso. Células malignas dificilmente podem ser consideradas como um melhoramento das similares normais. Elas são "mais eficientes" apenas em sua actividade de replicação, mas mesmo isso é apenas um uso exagerado de um mecanismo celular já existente. Em muitos outros sentidos importantes, elas possuem características degenerativas. Elas não mostram nenhum ganho de informação, mas geralmente uma perda ou desordem de funções.
Ainda mais estranhamente, o processo de degeneração de células cancerosas tem sido visto como uma forma Darwiniana de mutação Mais uma vez, essa ideia falha em se sustentar quando submetida a um exame mais minucioso. Células malignas dificilmente podem ser consideradas como um melhoramento das similares normais. Elas são "mais eficientes" apenas em sua actividade de replicação, mas mesmo isso é apenas um uso exagerado de um mecanismo celular já existente. Em muitos outros sentidos importantes, elas possuem características degenerativas. Elas não mostram nenhum ganho de informação, mas geralmente uma perda ou desordem de funções.
Em toda essa investigação, nenhuma mutação que tenha aumentado a eficiência de uma proteína humana geneticamente codificada foi encontrada.
.
As mutações comportam-se como um "atirador cego", um destruidor que dispara aleatoriamente suas "balas" mortais em direcção aos modelos tão bem projectados de mecanismos moleculares viventes.
(…)
Esta pesquisa realça a assustadora realidade da futura desesperança da raça humana sem a intervenção salvadora de Deus e de Seu Cristo. As mutações lentamente continuam a nos prejudicar. Cada geração tem uma constituição genética levemente mais desordenada do que a precedente, e nenhuma quantidade de eugenia pode reverter esse processo de deterioração. A terapia génica pode mascarar os efeitos, mas não irá reverter o processo degenerativo básico.
Esta pesquisa realça a assustadora realidade da futura desesperança da raça humana sem a intervenção salvadora de Deus e de Seu Cristo. As mutações lentamente continuam a nos prejudicar. Cada geração tem uma constituição genética levemente mais desordenada do que a precedente, e nenhuma quantidade de eugenia pode reverter esse processo de deterioração. A terapia génica pode mascarar os efeitos, mas não irá reverter o processo degenerativo básico.
.
Eventualmente as mutações irão transformar o código genético humano em uma mensagem inteligível.
.
Uma ligeira, porém definida e contínua taxa de mutação, acompanhada de uma taxa nula de mudanças genéticas positivas irá eventualmente transformar o código genético humano em uma mensagem inteligível. O problema é como um grande livro, escrito com uma gramática perfeita a princípio, mas com substituições aleatórias das letras introduzidas num ritmo contínuo. O livro ainda permanecerá legível por algum tempo, mas finalmente irá perder todo o sentido. Assim como o universo é projectado para alcançar um estado de máxima entropia, a raça humana também está condenada a uma morte degenerativa, não apenas como indivíduos, mas como um todo.

Nenhum comentário:
Postar um comentário